
背景介绍:手性γ-酮酯及其衍生物广泛存在于天然产物、药物和农用化学品中,是重要的有机合成砌块。从简单易得的原料出发高效、高对映选择性地合成这类分子仍具挑战。钯催化的不对称酰基羰基化反应是同时向烯烃引入两个不同羰基的理想策略,已报道的方法主要局限于分子内的三组分反应。由于酰基-钯(II)物种对烯烃的反应性较低,实现烯烃的分子间不对称四组分酰基羰基化反应此前尚未报道。针对上述问题,西南大学化学化工学院李响教授课题组提出了在一种温和条件下,通过富电子吡啶-噁唑啉(Pyox)配体调控反应的化学选择性和对映选择性,实现钯催化烯烃、双芳基碘鎓盐、CO和甲醇的四组分不对称反应直接合成手性γ-酮酯的方法(文章连接:https://doi.org/10.1021/jacs.6c04152)。
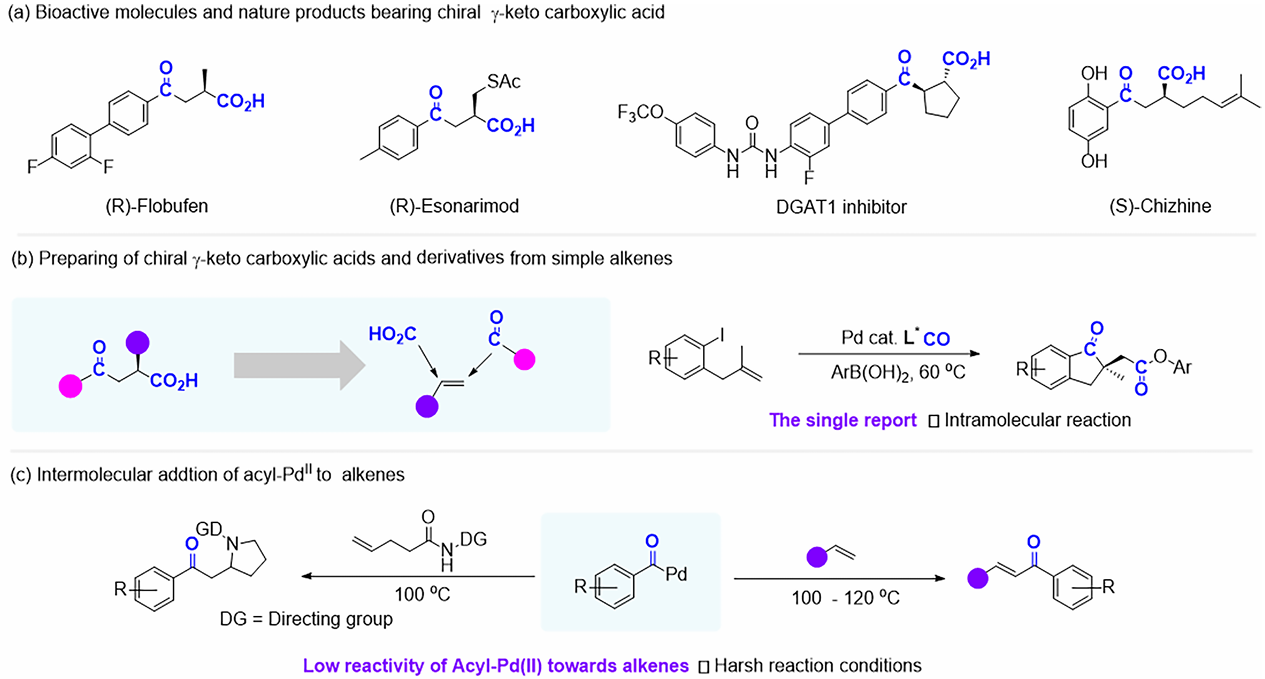
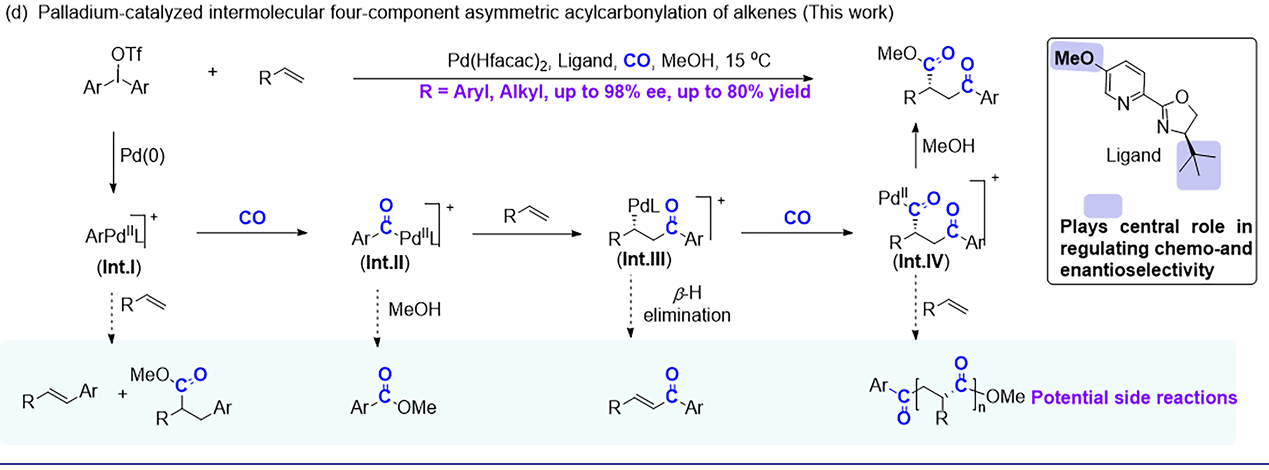
课题思路:作者提出,通过双芳基碘鎓盐对Pd(0)氧化加成,并经历CO迁移插入,可以生成阳离子型酰基-钯(II)物种。与中性物种相比,阳离子型酰基-钯(II)具有更强的π-亲电性,在合适手性配体存在下,与烯烃发生对映选择性反应。随后经历β-酰基-钯(II)物种的进一步羰基化,最终生成目标手性γ-酮酯。整个反应设计的关键在于通过配体调控反应中可能存在的多种竞争副反应路径(如Heck反应、醇解、β-氢消除、烯烃与CO多聚等),从而实现高的化学选择性和对映选择性。
底物拓展与应用: 该反应对脂肪族烯烃具有广泛的普适性。对各种官能团如亚胺、酮、卤素、酰胺、酯、醚、碳酸酯、砜、硝基、氰基、香豆素、含氮、氧杂环底物以及ciprofibrate, estrone, andibuprofen等天然产物和药物的烯烃衍生物均能良好兼容,并以中等至良好的收率(50%-80%)和优秀的对映选择性(up to 98%)拓展得到了55个相应产物。在放大反应中,以良好收率和高对映选择性得到产物。该反应还展示了良好的合成应用价值,所得手性γ-酮酯可作为多功能合成砌块,通过Wittig-Horner反应、Grignard加成、NaBH4还原、Baeyer-Villiger氧化、Schmidt重排等一系列转化,高效构建α,β-不饱和酯、手性内酯、内酰胺、β-酰基脲等复杂分子。同时还成功合成生物活性天然产物(−)-tetrahydro lipstatin和药物分子((S)-mitiglinide,一种II型糖尿病治疗剂)关键中间体,凸显了该方法的实用性。
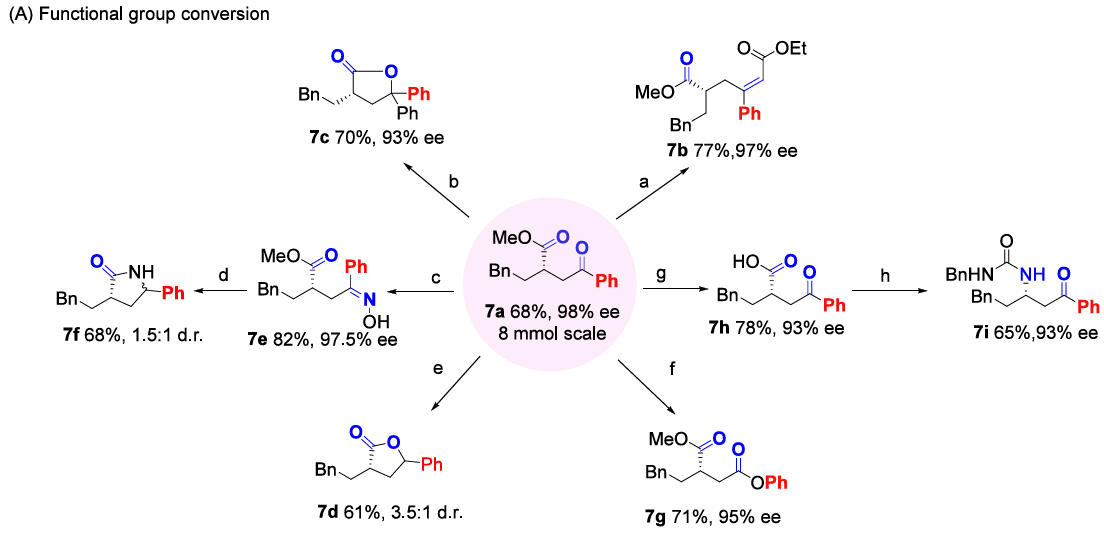
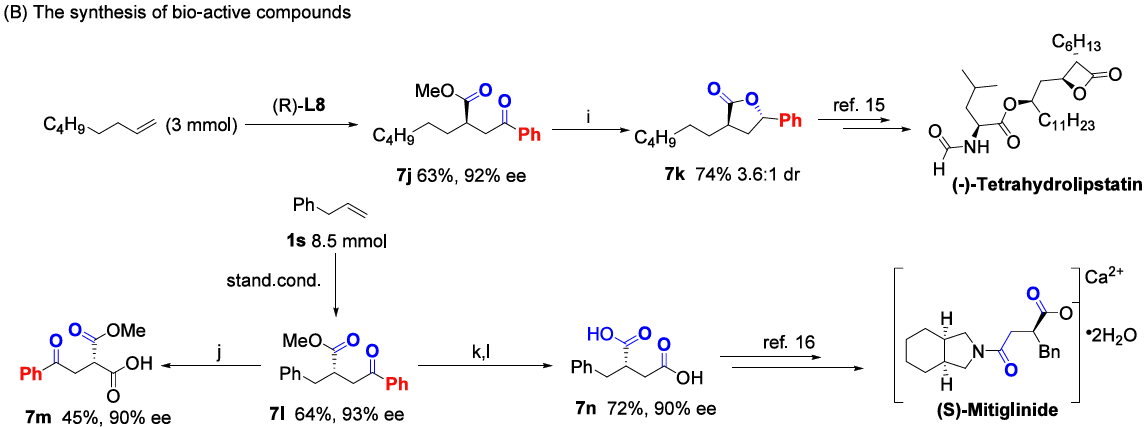
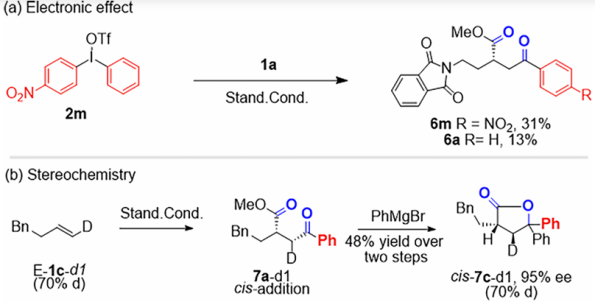
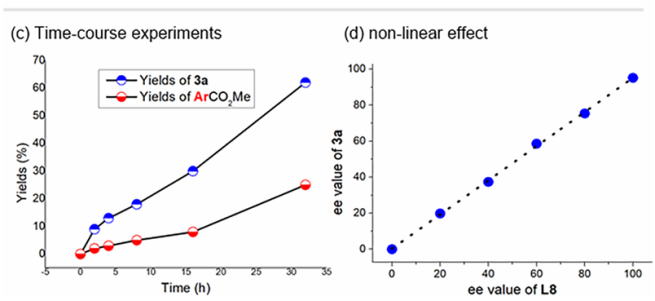
机理探究:机理研究表明,在用非对称双芳基碘鎓盐时,反应优先在缺电子芳基一侧发生,证实了双芳基碘鎓盐对Pd(0)的氧化加成是反应的启动步骤。产物立体化学分析表明,酰基和酯基是顺式加成到烯烃双键上的,这与烯烃对酰基-钯(II)迁移插入、随后CO对sp³烷基-钯(II)插入的过程一致。动力学实验表明,反应初期芳基酰基-钯物种更倾向于与烯烃发生迁移插入,而非直接与甲醇反应。非线性效应实验显示产物对映体过量值与配体对映体纯度呈线性关系。
总结:作者成功开发了一种通用的模块化钯催化策略,实现了简单烯烃的不对称分子间四组分酰基羰基化反应,为从丰富烯烃原料直接合成高附加值的手性γ-酮酯提供了直接途径。该反应的关键在于利用富电子的Pyox配体,有效提升了阳离子型酰基-钯物种对烯烃的反应性,并精准调控了反应的化学选择性和对映选择性。该方法条件温和,底物适用范围广,官能团兼容性好,对映选择性优异,具有重要的合成应用价值。
西南大学化学化工学院博士生周韦为该文章的第一作者,李响教授为通讯作者,西南大学化学化工学院为通讯单位,这项工作得到了国家自然科学基金项目(22401239)的支持。
